Авторы: К.Ю. Клышников, Е.А. Овчаренко, В.И. Ганюков, Р.С. Тарасов, А.Н. Коков, Л.С. Барбараш
Ключевые слова: метод конечных элементов; транскатетерная имплантация аортального клапана; трехмерные модели биологических объектов.
Цель исследования
Разработать метод равномерного дробления для построения расчетной сетки трехмерных моделей биологических объектов при моделировании транскатетерной имплантации аортального клапана на основе медицинских DICOM-изображений с использованием математических методов обработки и оценить его эффективность в сравнении с типовыми подходами: методом полигонов и САПР-методом.
Материалы и методы
Отработку методов реконструкции осуществляли на примере клинических данных пациента Н., 68 лет, перенесшего транскатетерное протезирование клапана аорты. Входными данными явились результаты мультиспиральной компьютерной томографии. Реконструкцию биологических объектов (корня аорты) проводили тремя методами: методом полигонов (Mimics, Бельгия), САПР-методом (NX 9.0, Германия) и с помощью авторского алгоритма, реализованного в среде MATLAB (США). Численное моделирование как один из критериев качества полученных реконструированных моделей выполняли в среде инженерного анализа Abaqus/CAE 6.14 (США) с воспроизведением условий нагружения моделей физиологическим давлением в два этапа: в систолу и диастолу.
Результаты
Оценка реконструированных моделей корня аорты показала, что предлагаемый численный метод позволяет сегментировать объект (корень аорты) на более однородные элементы по сравнению с методом полигонов и САПР-методом. Так, в случае метода полигонов использовали 128 452 тетраэдра (пирамиды, C3D4); в случае САПР-метода — 28 456 гексаэдров (параллелограммы, С3D8); в случае численного метода — 24 644 аналогичных C3D8 элемента. Результаты численного моделирования также разнились: в случае метода полигонов максимум напряжения по Мизесу составил 0,262 МПа; для САПР-алгоритма — 0,412 МПа, в случае численного метода — 0,359 МПа. Важным критерием эффективности реконструкции явилось время расчета: для метода полигонов — 458,6 с, в случае САПР-алгоритма — 377,2 с (на 21,5% меньше), в случае предложенного численного метода — 341,8 с (на 34,1% меньше).
Заключение
Полученные качественные и количественные результаты проведенного исследования демонстрируют эффективность применения предложенного алгоритма реконструкции биологических объектов на основе DICOM-файлов для задач численного анализа. Использование данного алгоритма при моделировании транскатетерной имплантации аортального клапана дает возможность сократить время численного анализа и повысить его точность, что позволит улучшить качество и увеличить скорость предоперационного планирования.
Введение
Одной из важнейших задач кардиохирургии является предоперационное планирование вмешательств — подбор доступов, выбор протеза, а также прогнозирование исходов и осложнений с целью выработки стратегии их минимизации [1, 2]. Особую актуальность планирование имеет для малоинвазивных операций, при которых интервенционный кардиолог вынужден оценивать характер и объем поражения только по результатам инструментальных исследований — эхокардиографии (эхоКГ), мультиспиральной компьютерной томографии (МСКТ), МРТ [3–5]. К подобным вмешательствам относят инновационное направление в международной медицине — чрескожное протезирование митрального клапана и транскатетерные имплантации аортального клапана (ТИАК), получившие значительное распространение в последнее десятилетие в России [6–8]. Опираясь на собственный опыт, требования производителя и регулятора, протоколы обществ кардиологов, клиницист планирует ТИАК-вмешательство, точный исход которого определится только по итогам выполнения процедуры, что вносит элемент неопределенности, который проявляется типовыми осложнениями для подобных процедур: парапротезной фистулой и нарушением проводимости [9], возникающими вследствие погрешностей позиционирования и несоответствия типоразмера протеза. Современные численные методы, вошедшие в инструментарий разработки и тестирования медицинских изделий, рассматриваются в качестве перспективной технологии при прогнозировании ТИАК за счет возможностей моделирования процедуры имплантации разных устройств и их типоразмеров [10, 11]. В литературе появляются работы с описанием численного анализа ТИАК, однако недостаточный уровень прогностической точности и высокая трудозатратность метода не позволяют использовать его в клинике, вследствие чего исследования носят лишь единичный экспериментальный характер [12, 13].
Возможной причиной ограниченности применения численных методов при ТИАК-планировании также может являться качество трехмерных моделей объектов, участвующих во взаимодействии — корня аорты, протеза клапана, нативного клапана аорты, кальцинатов и дегенеративных элементов. Существующий метод неразрушающего исследования структуры объектов — компьютерная микротомография — позволяет с высокой точностью (до 0,025 мм) воссоздать структуру протеза ТИАК и провести его реконструкцию [14], однако ввиду высокой лучевой нагрузки невозможно их применение на живых организмах, поэтому в случае предоперационного планирования доступно использование только «классических» методов клинической визуализации — МСКТ, МРТ, эхоКГ.
Реконструкция трехмерных компьютерных моделей для планирования ТИАК должна удовлетворять комплексу требований: высокая точность, малое время вычисления, валидность с медицинской точки зрения [15]. В современной практике реконструкции используют два основных подхода: наиболее распространенный метод полигонов, реализованный в коммерческих ПО (Amira; Mimics; Slicer 3D), и САПР-метод на основе систем автоматизированного проектирования (NX; SolidWorks). Выбор того или иного метода зависит от требуемой точности и сложности модели, однако каждый из них обладает собственными недостатками, сказывающимися в итоге на результатах моделирования. Метод полигонов демонстрирует высокую точность моделей, которая сопряжена с большим количеством элементов узлов сетки, значительно усложняющим компьютерный расчет [16, 17]. САПР-метод, напротив, позволяет создавать качественные сетки, но значительно более трудозатратен и обладает более низкой точностью моделей
Материалы и методы
DICOM-данные. В качестве объекта для отработки методов реконструкции трехмерных моделей при численном анализе ТИАК-процедуры использовали в формате DICOM (отраслевой стандарт создания, хранения, передачи и визуализации цифровых медицинских изображений и документов — Digital Imaging Communications in Medicine) снимки пациента Н., 68 лет, которому была проведена процедура с применением коммерческого биопротеза CoreValve (Medtronic Inc., США). Согласно протоколу, на предоперационном этапе планирования пациенту выполняли МСКТ без использования контраста с визуализацией в систолу и диастолу при помощи клинического томографа SOMATOM Sensation 64 (Siemens, Германия). Направление сканирования — краниокаудальное со следующими характеристиками: напряжение — 120 кВ, апертура — 200 мм, питч-фактор — 0,7 мм, разрешение — 0,625 мм, наличие ЭКГ-синхронизации, толщина среза — 1 мм.
Реконструкция трехмерной геометрии — метод полигонов. На основании полученных изображений (см. «DICOM-данные») была проведена реконструкция корня аорты с помощью коммерческого ПО для работы с медицинскими изображениями — методом полигонов. Для этого наборы изображений импортировали в программу обработки медицинских изображений Mimics (Materialise, Бельгия), где с использованием встроенных инструментов по выделению контуров проводили реконструкцию корня аорты. Полученную трехмерную реконструкцию экспортировали в качестве конечно-элементной сетки в виде файла, адаптированного для импорта в среду инженерного анализа Abaqus/CAE 6.14 (Dassault Systèmes, США).
Реконструкция трехмерной геометрии — САПР-метод. Полученные сеты DICOM-изображений разделяли на отдельные изображения с сохранением исходного качества. Среди них условно выделяли группу «базовых» и «направляющих» срезов (рис. 1, а, г). «Базовые» срезы соответствовали аксиальной плоскости МСКТ, т.е. располагались вдоль основного объекта реконструкции — корня аорты. Частота изображения зависела от исходной сложности участка реконструируемого объекта. Так, синусы Вальсальвы, устья коронарных артерий и фиброзное кольцо клапана аорты, представляющие наибольший интерес в прогностическом плане, были реконструированы значительно детальнее, чем восходящий отдел (рис. 1, б). «Направляющие» срезы соответствовали сагиттальной плоскости и двум вспомогательным плоскостям, проходящим через условную продольную ось корня аорты. Данные срезы предназначены для выделения внутреннего и внешнего профилей объекта и построения его «скелета». Выделенные таким образом изображения импортировали в САПР NX 9.0 (Siemens PLM Software, Германия) с сохранением взаимного расположения и масштаба, определяемого разрешающей способностью клинического МСКТ (см. рис. 1, б, д).

Импортированные изображения легли в основу эскизов, которые были построены в плоскостях, соответствующих «базовым» и «направляющим» срезам. Построение эскизов осуществляли средствами САПР с использованием дуг, отрезков и разомкнутых сплайнов с формированием замкнутых контуров для внутренней и внешней поверхностей модели («базовые срезы»), а также разомкнутых «направляющих» кривых (рис. 1, в, е). Последовательное объединение элементов эскизов в тонкостенные оболочки средствами САПР позволило получить набор мембран, описывающих реконструируемую геометрию. Последующая «сшивка» мембран в твердое тело сформировала требующуюся геометрию (рис. 1, ж, з).
Реконструкция трехмерной геометрии — метод равномерного дробления. В основе предлагаемого метода реконструкции корня аорты лежит последовательный анализ всех имеющихся DICOM-срезов с алгоритмическим построением гексагональной сетки конечных элементов. Полученный по данным МСКТ набор изображений импортировали в авторский скрипт среды MATLAB (MathWorks, США). Разработанный алгоритм предусматривает создание трехмерной матрицы чисел в виде оттенков серого с последующим аффинным преобразованием с целью позиционирования оператором области интереса относительно рабочей системы координат. Далее автоматически производится бинаризация по методу Оцу [18] (рис. 2, в). В каждом бинарном изображении автоматически генерировали стартовую точку, принадлежащую внутреннему просвету корня аорты. Начиная от данной стартовой точки автоматически производили обход контура с использованием алгоритма Мура таким образом, чтобы выделить границу внутреннего просвета корня аорты, основанную на разнице контраста, после чего определяется центр масс (рис. 2, г).

Найденный центр масс является началом лучей, используемых для поиска пересечений с границей внутреннего контура, которые направлены радиально с заданным шагом (в 1°). Найденные точки пересечения служат началом построения отрезков до ближайшего белого пикселя в радиальном направлении аналогично используемым ранее лучам. Данные отрезки являются искомой толщиной стенки аорты, т.е. основой для построения наружного контура модели. Однако не во всех случаях возможно достичь пересечения отрезков с белым пикселем, так как в результате бинаризации на отдельных томограммах получено черное пространство вплоть до границ изображения. В связи с этим массив отрезков — толщин — был дополнен в данных участках с использованием метода линейной интерполяции между двумя краевыми известными значениями в срезе и выражен в цилиндрической системе координат. Таким образом, на основании полученного контура внутреннего просвета корня аорты и полного массива отрезков — толщин — с шагом в 1° реконструируется наружный контур искомой модели. В дальнейшем задача сводится к определению координат узлов, которые легли в основу конечных элементов, описывающих стенку корня аорты: определяются координаты узлов в двух соседних срезах, после чего производится последовательное их объединение в формате, пригодном для импорта в среду инженерного анализа Abaqus/CAE 6.14, представленную в виде неродственной сетки типа исполняемого input-файла (см. рис. 2).
Численное моделирование. Для апробирования предложенного метода реконструкции в условиях численного эксперимента и оценки особенностей его применения проводили моделирование податливости стенки корня аорты в ответ на воздействие нормального физиологического давления: 120 мм рт. ст. для систолы и 80 — для диастолы. Численный эксперимент осуществляли методом конечных элементов в среде инженерного анализа Abaqus/CAE 6.14. В работе использовали три полученные модели корня аорты — методом полигонов, САПР-методом и предложенным методом равномерного дробления (рис. 3). На внутреннюю поверхность моделей прикладывали нагрузку типа «давление» с амплитудой, аналогичной давлению в корне аорты в норме. Граничные условия определяли путем наложения ограничений на перемещение вдоль центральной продольной оси (Z) в области фиброзного кольца и синотубулярного сочленения.
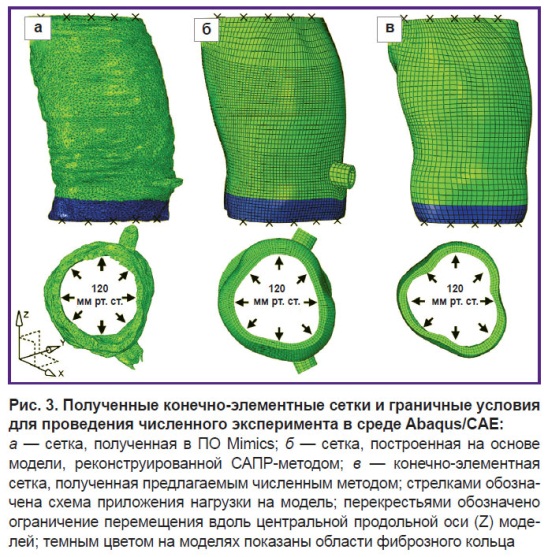
В качестве модели материала использовали данные собственных исследований физико-механических параметров нативного корня аорты трупного материала [19]. В результате были получены полиномиальные модели второго порядка гиперэластичных материалов для раздельного описания фиброзного кольца и вышележащих отделов аорты (см. рис. 3) со следующими коэффициентами (см. таблицу).
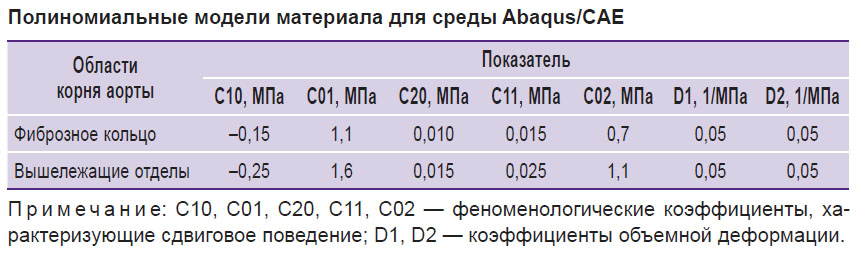
Прилагаемая на исследуемые объекты нагрузка являлась псевдодинамической вследствие низких скоростей роста давления от систолы к диастоле, поэтому в качестве решателя выбрали Abaqus/Standard, не подразумевающую явного интегрирования по времени. В ходе моделирования оценивали напряженно-деформированное состояние: напряжение по Мизесу и показатель логарифмической деформации, а также качественное их распределение на соответствующих эпюрах.
Результаты и обсуждение
Результаты реконструкции моделей корня аорты показали, что предлагаемый метод равномерного дробления позволяет сегментировать объект — корень аорты — на более однородные элементы по сравнению с методом полигонов и САПР-методом. При этом из литературы известно, что недостаточная однородность может отрицательно повлиять на результаты моделирования и исказить их [20]. Полученные нами данные служат подтверждающим фактом данной особенности численных методов. Так, в случае использования моделей корня аорты на основе разработанного алгоритма и САПР-метода отсутствовали участки высокого градиента напряжения по Мизесу, в то время как при полигональной модели такие области наблюдались. Стоит отметить, что возникновение высокого градиента между конечными элементами может являться следствием ошибки расчета, так как не имеет физического объяснения — в однородном материале не может возникать значимого градиента напряжения в двух соседних точках. Таким образом, число ошибок расчетов при использовании предложенного метода и САПР-метода реконструкции оказалось значительно ниже.
В целом в численном эксперименте получены вариативные данные для количественных результатов. Так, в случае метода полигонов максимум напряжения по Мизесу составил 0,262 МПа; для САПР-алгоритма — 0,412 МПа, в случае метода равномерного дробления — 0,359 МПа. Следует обратить внимание, что используемые гексаэдрические элементы в случае САПР и предложенного метода демонстрируют в целом схожие результаты, в то время как сетка, полученная в ПО Mimics, несколько занижает оценку напряженно-деформированного состояния (рис. 4).
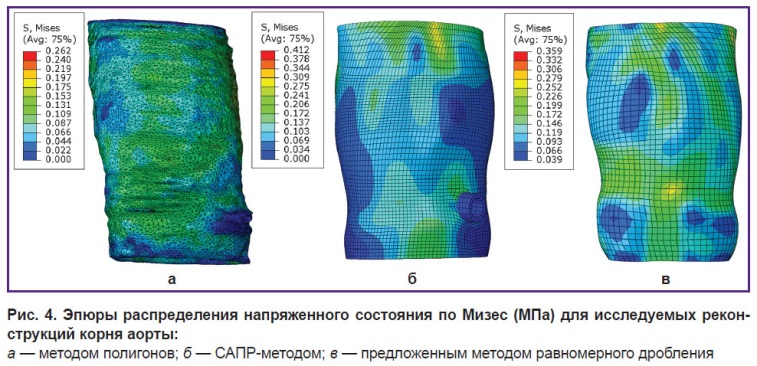
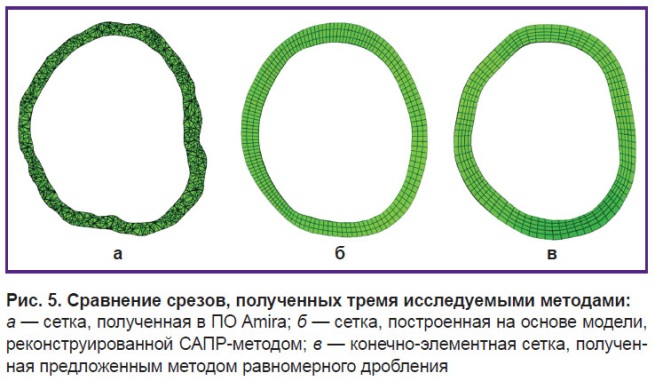
Важным параметром с точки зрения моделирования является время расчета, т.е. непосредственное физическое время, затраченное решателем на численный эксперимент. В проведенном исследовании показано, что даже в случае относительно простой задачи — моделирования действия давления на корень аорты — получаются значимые различия между моделями, использующими описанные подходы к реконструкции. Так, в случае метода полигонов время расчета составило 458,6, а в случае САПР-алгоритма — 377,2 (на 21,5% меньше), в случае метода равномерного дробления — 341,8 (на 34,1% меньше). Обусловлено данное различие типом конечных элементов, потребовавшихся для описания полученных моделей, и их количеством при сохранении равной длины ребра. Так, в случае метода полигонов использовали 128 452 тетраэдра (пирамиды — C3D4); в случае САПР-метода — 28 456 гексаэдров (параллелограммы — С3D8); в случае численного метода — 24 644 аналогичных C3D8 элемента (см. рис. 3). Средняя длина ребра составила 0,99; 0,91 и 0,98 мм соответственно. С другой стороны, использование тетраэдров не лишено смысла: тетраэдрические сетки способны описывать любую геометрию, в то время как гексаэдрические требуют определенной длительной предподготовки моделей как в случае САПР-метода, так и в случае численного алгоритма. Различия точности полученных моделей на примере одного среза (выше синусов Вальсальвы) наглядно демонстрирует рис. 5. Видно, что, несмотря на общее сохранение геометрии среза, САПР-метод (рис. 5, б) грубо описывает реконструируемую область — сглаживая часть рельефа. Предлагаемый численный метод (рис. 5, в) также не лишен данного недостатка, однако в большей степени соответствует сетке, построенной методом полигонов (рис. 5, а).
Баланс «качество–стоимость» обусловлен требованиями и сложностью численного эксперимента, однако в случаях многокомпонентного взаимодействия (например, прогнозирование исходов ТИАК) оба подхода (САПР и численный) представляются рациональными, так как позволяют значительно экономить время наиболее «затратной» части работы — непосредственно моделирования.
Заключение
Полученные качественные и количественные результаты проведенного исследования демонстрируют эффективность применения предложенного метода реконструкции биологических объектов для задач численного анализа. Возможность использования более «практичных» конечных элементов (гексаэдров), меньшего их количества, с более качественным — однородным — построением модели понижает временные затраты на проведение численного анализа ТИАК и повышает его точность.
Финансирование исследования
Работа выполнена при поддержке поискового научного исследования №0546-2017-0004 «Разработка новых технических, тактических и стратегических подходов к эндоваскулярной диагностике и лечению атеросклероза», реализуемого на базе НИИ комплексных проблем сердечно-сосудистых заболеваний (Кемерово).
Литература:
- Sardari Nia P., Heuts S., Daemen J., Luyten P., Vainer J., Hoorntje J., Cheriex E., Maessen J. Preoperative planning with three-dimensional reconstruction of patient’s anatomy, rapid prototyping and simulation for endoscopic mitral valve repair. Interact Cardiovasc Thorac Surg 2017; 24(2): 163–168, https://doi.org/10.1093/icvts/ivw308.
- Sindeev S.V., Frolov S.V. Modeling the hemodynamics of the cardiovascular system with cerebral aneurysm. Math Models Comput Simul 2017; 9(1): 108–119, https://doi.org/10.1134/s2070048217010148.
- Kilic T., Yilmaz I. Transcatheter aortic valve implantation: a revolution in the therapy of elderly and high-risk patients with severe aortic stenosis. J Geriatr Cardiol 2017; 14(3): 204–217, https://doi.org/10.11909/j.issn.1671-5411.2017.03.002.
- Богачев-Прокофьев А.В., Шарифулин Р.М., Зубарев Д.Д., Журавлева И.Ю., Караськов А.М. Непосредственные результаты транскатетерного протезирования аортального клапана трансаортальным доступом. Российский кардиологический журнал 2017; 8: 51–58, https://doi.org/10.15829/1560-4071-2017-8-51-58.
- Chaturvedi A., Hobbs S.K., Ling F.S., Chaturvedi A., Knight P. MRI evaluation prior to transcatheter aortic valve implantation (TAVI): when to acquire and how to interpret. Insights Imaging 2016; 7(2): 245–254, https://doi.org/10.1007/s13244-016-0470-0.
- Бокерия Л.А., Алекян Б.Г., Пурсанов М.Г., Мироненко В.А., Бокерия О.Л., Макаренко В.Н., Захарченко А.В., Косенко А.И., Базарсадаева Т.С., Сандодзе Т.С., Алехина М.А. Транскатетерная имплантация аортального клапана: первый опыт в России. Грудная и сердечно-сосудистая хирургия 2011; 2: 4–10.
- Бокерия Л.А., Гудкова Р.Г. Сердечно-сосудистая хирургия — 2015. Болезни и врожденные аномалии системы кровообращения. М: НЦССХ им. А.Н. Бакулева; 2016; 208 с.
- Журавлева И.Ю., Богачев-Прокофьев А.В., Демидов Д.П., Караськов А.М. Транскатетерное протезирование митрального клапана: современное состояние проблемы. Кардиология 2017; 57(8): 51–59, https://doi.org/10.18087/cardio.2017.8.10018.
- Neragi-Miandoab S., Michler R.E. A review of most relevant complications of transcatheter aortic valve implantation. ISRN Cardiol 2013; 2013: 956252, https://doi.org/10.1155/2013/956252.
- Jung J.I., Koh Y.S., Chang K. 3D printing model before and after transcatheter aortic valve implantation for a better understanding of the anatomy of aortic root. Korean Circ J 2016; 46(4): 588–589, https://doi.org/10.4070/kcj.2016.46.4.588.
- Tzamtzis S., Viquerat J., Yap J., Mullen M.J., Burriesci G. Numerical analysis of the radial force produced by the Medtronic-CoreValve and Edwards-SAPIEN after transcatheter aortic valve implantation (TAVI). Med Eng Phys 2013; 35(1): 125–130, https://doi.org/10.1016/j.medengphy.2012.04.009.
- Wald S., Liberzon A., Avrahami I. A numerical study of the hemodynamic effect of the aortic valve on coronary flow. Biomech Model Mechanobiol 2017; 17(2): 319–338, https://doi.org/10.1007/s10237-017-0962-y.
- Bianchi M., Marom G., Ghosh R.P., Fernandez H.A., Taylor J.R. Jr., Slepian M.J., Bluestein D. Effect of balloon-expandable transcatheter aortic valve replacement positioning: a patient-specific numerical model. Artif Organs 2016; 40(12): E292–E304, https://doi.org/10.1111/aor.12806.
- Клименов В.А., Алхимов Ю.В., Штейн А.М., Касьянов С.В., Бабиков С.А., Батранин А.В., Осипов С.П. Применение и развитие методов цифровой радиографии для технической диагностики неразрушающего контроля и инспекции. Контроль. Диагностика 2013; 13: 31–42.
- Raut S.S., Liu P., Finol E.A. An approach for patient-specific multi-domain vascular mesh generation featuring spatially varying wall thickness modeling. J Biomech 2015; 48(10): 1972–1981, https://doi.org/10.1016/j.jbiomech.2015.04.006.
- Pavarino E., Neves L.A., Machado J.M., de Godoy M.F., Shiyou Y., Momente J.C., Zafalon G.F., Pinto A.R., Valêncio C.R. Free tools and strategies for the generation of 3D finite element meshes: modeling of the cardiac structures. Int J Biomed Imaging 2013; 2013: 540571, https://doi.org/10.1155/2013/540571.
- Yu Z., Wang J., Gao Z., Xu M., Hoshijima M. New software developments for quality mesh generation and optimization from biomedical imaging data. Comput Methods Programs Biomed 2014; 113(1): 226–240, https://doi.org/10.1016/j.cmpb.2013.08.009.
- Otsu N. A threshold selection method from gray-level histograms. IEEE Trans Syst Man 1979; 9: 62–66, https://doi.org/10.1109/tsmc.1979.4310076.
- Овчаренко Е.А., Клышников К.Ю., Глушкова Т.В., Бураго А.Ю., Журавлёва И.Ю. Нелинейная изотропная модель корня аорты человека. Технологии живых систем 2014; 11(6): 43–47.
- Krishnamurthy A., Gonzales M.J., Sturgeon G., Segars W.P., McCulloch A.D. Biomechanics simulations using cubic hermite meshes with extraordinary nodes for isogeometric cardiac modeling. Comput Aided Geom Des 2016; 43: 27–38, https://doi.org/10.1016/j.cagd.2016.02.016.
Источник: научно-практический журнал "СТМ" 2018 – том 10, №4