Автор: Резник Н.Л., к.б.н.
Лептиновое бесчувствие
Фантасты шутят, что в будущем медицина победит все болезни, кроме насморка. К сожалению, в наше время список трудноизлечимых недугов куда длиннее, и один из них — ожирение. От него страдают сотни миллионов человек, оно чревато многими тяжелейшими последствиями, а лекарства от этой беды нет.


В 1995 году у медиков и их тучных пациентов появилась надежда. Джеффри Фридман, руководитель лаборатории молекулярной генетики Медицинского института Говарда Хьюза, и его сотрудники обнаружили гормон лептин, который синтезируют клетки жировой ткани адипоциты. Этот гормон связывается с рецепторами в клетках центральной нервной системы, в том числе гипоталамуса, снижает чувство голода и стимулирует высвобождение энергии, запасенной в жировой ткани, то есть «сгорание» жиров. Чем больше масса жировой ткани, тем больше лептина она синтезирует. Гормон подает сигналы мозгу, млекопитающее меньше ест, расходует жир, уровень лептина в крови падает, аппетит растет. Этот механизм позволяет организму поддерживать относительно постоянный запас энергии. Специалисты довольно быстро обнаружили ген ОВ, кодирующий лептин, и ген лептинового рецептора DB. Мутантные мыши ob/ob лишены гормона, безрецепторные мутанты db/db не воспринимают его сигналы. В обоих случаях животные не в состоянии контролировать аппетит и энергообмен, и у них развивается сильнейшее ожирение.


Лептин поначалу показался идеальным похудательным средством: принял его, и есть не хочется. Тем более что в отличие от голодания, которое вызывает потерю мышечной массы, от лептиновой терапии рассасывается только жир. Но этим чаяниям не суждено было сбыться: экзогенный лептин вызывал снижение аппетита и веса у мышей с нормальной массой тела, но не действовал на грызунов, раскормленных жирной пищей. Уже в 2004 году Джеффри Фридман с коллегами установил, что при ожирении, которое вызвано избыточным питанием и не связано с генетическими дефектами, лептин не в состоянии ни подавить чувство голода, ни повысить расход энергии, хотя его концентрация в крови очень высока. Вместо этого для ожирения характерны гиперфагия, сиречь обжорство, и сберегание жира, как при дефиците лептина. Это открытие привело команду Фридмана к выводу, что в состоянии ожирения организм клептину нечувствителен. Однако более убедительных доказательств они не представили, что вызвало среди научной общественности долгие дебаты о том, существует ли на самом деле устойчивость к лептину. Параллельно исследователи искали лекарство, которое повысило бы чувствительность к гормону, но так и не нашли.
Этими поисками давно занимается Умут Озкан, возглавляющий лабораторию в Гарвардской медицинской школе, его сотрудники и постдоки. Исследователи выяснили, что развитию ожирения сопутствует хронический стресс эндоплазматического ретикулума (ЭР-стресс). Придется сказать о нем несколько слов.
Эндоплазматический ретикулум — сложная внутриклеточная структура, сеть вакуолей и канальцев, ограниченных мембраной. На мембране происходит синтез белков, которые затем поступают в просвет сети, где происходит их модификация и укладывание в третичную структуру. Готовые белки выходят из ЭР и перемещаются к месту назначения. Если белок по какой-то причине не сложился в функционально-активную форму, он остается в просвете ЭР, пока не примет нужную конформацию или не будет выведен оттуда на деградацию.
Но иногда белков скапливается слишком много, они забивают ретикулум и приводят его в стрессовое состояние. Клетка в ответ запускает каскад реакций, призванных исправить положение. При этом изменяется активность многих генов, регулирующих в том числе такие жизненно важные процессы, как воспаление, метаболические нарушения и даже апоптоз. Если не удается быстро справиться сЭР-стрессом и он переходит в хроническую форму, организм заболевает (рис. 1).
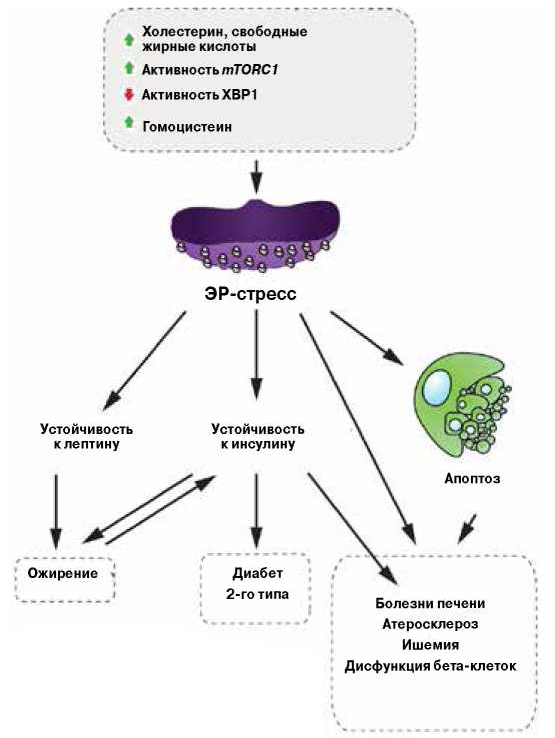
Рис.1. Реакция на ЭР-стресс в клетках гипоталамуса вызывает устойчивость к инсулину и лептину, а в последствии ожирение, диабет 2-го типа, различные метаболические болезни печени и сердечно-сосудистые заболевания.
Стресс возникает по разным причинам: усиленный белковый синтез, мутации, вызывающие дефект складывания; изменение концентрации некоторых метаболитов, в том числе избыток холестерина, свободных жирных кислот или аминокислоты гомоцистеина (он образуется после употребления мясных продуктов); недостаток белкаХВР1 в нейронах, то есть пониженная активность соответствующего гена; хроническая активация гена mTORCI, вызывающая невосприимчивость клеток к различным сигналам, в том числе инсулиновому. Между прочим, один из активаторов mTORCI — избыток пищи. Хронический ЭР-стресс в клетках гипоталамуса вызывает устойчивость клептину и, следовательно, ожирение.
Обнаружив связь между ЭР-стрессом, устойчивостью к лептину и ожирению, исследователи решили, что именно стресс — причина всех бед. Победив его, можно вернуть раздавшемуся организму чувствительность клептину, а вслед за тем и нормальный вес, вопрос лишь в том, как это сделать.


У организма есть несколько путей смягчения стресса, в том числе он задействует белки шапероны, которые способствуют складыванию белков, стабилизируют их конформацию и способствуют их выходу из ЭР. Существуют также химические шапероны — низкомолекулярные соединения, которые действуют сходным образом. Озкан и его сотрудники попытались полечить ожиревших мышей двумя такими соединениями: тауроурсодеоксихолиновой кислотой (TUDCA) и 4-фенил-бутиратом (4-РВА). Они действительно несколько смягчали ЭР-стресс в гипоталамусе грызунов и увеличивали их чувствительность клептину, но не очень сильно. Чтобы эффект был ощутим, нужны слишком высокие дозы. Следовательно, известные на данный момент химические шапероны не могут служить лекарством и надо искать новые соединения.
Ловля целастрола
Существует ли молекула, подходящая для данного случая, если да, то как ее выудить из безбрежного моря других молекул? Задача кажется неразрешимой, однако специалисты давно занимаются подобными поисками, так что у них уже есть неплохой задел. Например, в американском Институте Брода собрали данные о том, как меняется активность генов в различных культурах клеток человека, обработанных малыми молекулами, как синтезированными, так и природного происхождения. К этому массиву данных прилагаются программы для его анализа.
Приступив к поискам антистрессовой молекулы, Умут Озкан и его коллеги сначала выяснили, каков профиль экспрессии генов в печени и гипоталамусе нормальных мышей («Cell», 2015,161, 999—1011, doi: 10.1016/j.cell.2015.05.011). Затем они взяли лишенных лептина тучных мышей ob/ob и контрольных животных нормальной комплекции, ввели им химический шаперон 4-РВА или ген X6P/S в хвостовую вену. И ген, и шаперон смягчают последствия ЭР-стресса, но механизмы при этом задействованы разные. Разумеется, все необходимые контроли ученые тоже поставили. Затем они выделили микропробы РНК из печени и гипоталамуса мышей и получили профили экспрессии разных генов в тканях, пребывающих в нормальном состоянии, испытывающих ЭР-стресс и получающих разные лекарства от стресса. Особенно исследователей интересовало, как в разных условиях изменяется конформация белков, как проходит их складывание. В результате они получили представление о том, экспрессию каких генов надо изменить, чтобы стрессированные клетки пришли в нормальное состояние.
Составив список из нескольких десятков мышиных генов, наиболее значимых для преодоления ЭР-стресса, ученые нашли их человеческие аналоги, поскольку база данных Института Брода создана для тканей человека (для этого поиска использовали особую программу). И наконец, они смогли воспользоваться этой самой базой, чтобы выяснить, какие из известных малых молекул могут вызвать необходимые изменения генной экспрессии, если не точно такие же, то максимально близкие. Оказалось, что во всех случаях наиболее эффективная молекула одна и та же — целастрол, и она почти идеально удовлетворяет заданным условиям.

Рис.2. Триптеригиум Вильфорда – ядовитое растение с целебным корнем.
Целастрол не случайно оказался в базе данных. О нем европейская наука узнала, изучая китайскую народную медицину. Растения, которые она использует, нередко служат источником новых лекарств для медицины западной. Одно из хорошо известных растений — триптеригиум Вильфорда (Trypterygium wilfordii) из семейства бересклетовых (рис. 2). Иногда его называют «лоза бога грома». Сама лоза токсична, вещества, которые она содержит, даже в умеренных дозах могут вызвать расстройство желудка, головную боль, тошноту, в тяжелых случаях — бесплодие. Но китайские медики используют экстракт корня, тщательно следя, чтобы другие части растения в него не попали.


Экстракт корня назначают главным образом при ревматоидном артрите и других воспалительных заболеваниях. Корень содержит два основных активных компонента: триптолид и триптерин, также известный как целастрол. Этот пентациклический тритерпеноид рассматривают как перспективное противовоспалительное средство, его испытали на животных моделях артритов, волчанки, бокового амиотрофического склероза и даже болезни Альцгеймера. Он задерживает рост некоторых линий раковых клеток и опухолей у животных. Людей чистым целастролом лечить пока не пробовали. Сейчас молекулярные механизмы действия этого соединения активно изучают. Умут Озкан и его коллеги предположили, что целастрол может победить ЭР-стресс и вернуть тучному организму чувствительность к лептину.
Чувствительная стройность
Гипотезу проверяли, естественно, на мышах. Раскормленным животным ежедневно в течение трех недель внутрибрюшинно вводили целастрол, и за 15 дней их вес снижался с 47 до 35 г, после чего стабилизировался. Контрольные мыши, то есть толстушки, получавшие инъекции растворителя, не похудели. Потеря веса происходила за счет жира, содержание которого уменьшилось на 41,5% по сравнению с контрольной группой, а мышечная масса осталась неизменной. Помимо нормализации веса целастрол снижает уровень глюкозы в крови тучных животных и усиливает их чувствительность к инсулину (рис. 3).

Рис. 3. Целастрол смягчает ЭР-стресс клеток гипоталамуса и усиливает их чувствительность к лептину, благодаря чему нормализуется вес, обмен веществ и затраты энергии. Чтобы похудеть, нужны лептин и целастрол.
За первую неделю испытаний суточное потребление пищи у животных, получавших целастрол, сократилось с 2 г до 0,43 г, то есть на 79%. Но затем мышиный аппетит снова стал расти и к концу третьей недели практически восстановился. Эти колебания суточного потребления исследователи связывают с изменением концентрации лептина в плазме: все три недели она неуклонно снижалась и в конце срока оказалась почти на том же уровне, что и у мышей нормальной комплекции. Как мы помним, чем меньше в плазме лептина, тем сильнее аппетит. У ожиревших мышей уровень лептина был раз в 40 выше нормы, но они не реагировали на эту чудовищную концентрацию. После первых же инъекций к мышам будто вернулась чувствительность, и они почти перестали есть, пока уровень гормона не нормализовался. К этому времени животные и худеть закончили.
Исследователи предположили, что целастрол стимулирует потерю веса в основном в начале лечения, когда у тучных мышей уровень лептина в плазме высок, а когда он падает, действие целастрола почти неощутимо. Если эта гипотеза справедлива, препарат не должен влиять на мышей нормальной комплекции, поскольку лептина в их крови немного. И действительно, нормальные мыши от инъекций целастрола почти не худели, меньше есть не стали, уровень лептина у них не менялся, жир не «сгорал».
Эти данные еще более укрепили исследователей в мысли, что ожирение связано с потерей чувствительности к лептину, а целастрол эту чувствительность восстанавливает. Проанализировав уровень различных маркерных белков в гипоталамусе раскормленных мышей, ученые убедились, что целастрол существенно смягчает ЭР-стресс и нормализует работу лептиновых рецепторов.
Получается, что препарат позволяет похудеть не тем, кто имеет лишний вес, а тем, у кого в плазме избыток лептина. Если это предположение верно, то стройные мыши отощают, получив коктейль из лептина и целастрола. Так и оказалось. Лептин сам по себе вызывает потерю веса у мышей нормальной комплекции, после двух инъекций гормона они стали меньше есть и сбросили пол грамма. Получив оба препарата, они за два дня похудели почти на два грамма.
Смесь лептина и целастрола и с раскормленными мышами творит чудеса. Казалось бы, им дополнительный гормон не нужен, у них и своего немерено, однако прием лептина и целастрола позволил им потерять вес в два раза больший, чем курс одного целастрола. Потребление пищи у них тоже уменьшилось раза в два с половиной.
Для дальнейшего подтверждения своей гипотезы исследователи использовали ожиревших мутантных мышей, лишенных лептина (ob/ob) или рецептора к нему (db/db). На таких мышей целастрол почти не действует, потому что у одних нет гормона и не к чему повышать чувствительность, а другим нечем этот гормон чувствовать (см. рис. 3). В течение трехнедельного курса целастрола животные не худели и есть меньше не стали, напротив, продолжали медленно полнеть и к концу эксперимента набрали примерно 14% от исходной массы. Правда, безлептиновые мыши ob/ob в первые дни слегка похудели, потому что целастрол стимулирует выделение запасов энергии из жировой ткани, но этот эффект был слабым и недолгим. Очень быстро животные вернули утерянное и не отличались от контрольной группы. Инъекции лептина тоже действовали слабо. Зато целастрол в сочетании с лептином помог мутантам ob/ob вдвое уменьшить потребление пищи.
Исследователи пока не расшифровали полностью молекулярный механизм действия целастрола. Очевидно, он влияет на некоторые реакции, вызывающие ЭР-стресс. Как бы то ни было, целастрол имеет несомненный терапевтический потенциал в борьбе с ожирением и, возможно, с диабетом 2-го типа. Неприятно, конечно, лечиться уколами в живот, но ученые провели еще одну серию экспериментов, в которой целастрол вводили ожиревшим мышам не внутрибрюшинно, а через желудочный зонд (человек мог бы просто проглотить пилюлю). Такой способ введения оказался эффективнее инъекций, за три недели мыши сбросили более 45% веса. Эффект целастрола на 35—40% превышает результат, который можно получить хирургическими методами лечения ожирения. А еще ученые выяснили, что мыши могут принимать целастрол более шести месяцев, поедая при этом жирную пищу, и не толстеют, и никаких вредных побочных эффектов при этом не испытывают. Вот бы и людям так же повезло!
Источник: научно-популярный журнал «Химия и жизнь – XXIвек», №7, 2015 г.